ガラスとは何か?
1. はじめに
ガラスは古くから人類の生活に深く結びついており、紀元前数千年の昔から天然ガラスである黒曜石が矢じりや刃物として使用されている。人類がガラスを作るようになったのは紀元前1600年頃とされており、現在ガラスの成形法として広く知られている"宙吹き"が考案されたのは1世紀頃とされている。ガラスの製造には高温での溶融のような操作が必要であり、この当時は製造の困難さからガラスは大変な貴重品であり、主に装飾品や工芸品として使用された。やがて耐火性の容器すなわち「坩堝」が発明され、宙吹きだけでなく延伸やプレス等の成形法が使えるようになり、さまざまな形状のガラスが得られるようになった。12世紀にはベニスでガラス技術が大きく開花し、その後ボヘミアなどにも伝えられ、その伝統は現在も受け継がれている。
今世紀に入ると平面性の良い板ガラスが安価に製造されるようになり、また機械によるガラスの宙吹きの進歩によって種々のガラス容器が簡単に製造できるようになった。
2. ガラスとは?
先に述べたように人類は古くからガラス加工に取り組んできたがガラスの本質が知られるようになったのは実は今世紀に入ってからである。
ガラスは見ての通り固体であるが、他の固体材料、例えば金属やセラミックスとは全く異なった構造を持つ。それはガラスが「非晶質」であり、他の固体材料は「結晶質」であることである。結晶質とはその物質を構成する原子(分子)が規則正しく配列した図1(b)のような構造を持つ。これは高温で液体であった物質が温度が下がるにつれ規則的な構造をとった方が安定になり、そのため凝固点において構成原子(分子)が再配列して結晶質となるためである。しかし液体の粘度が高い場合には冷却が速いと再配列に十分な時間がなく、図1(a)のように液体に似たランダムな構造をとる。これがガラスである。すなわち結晶は平衡状態にあるのに対し、ガラスは非平衡のまま液体が過冷却され、固体となったものである。この関係を図2に示す。
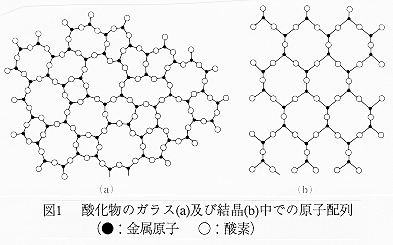
3. ガラスの特徴
先に述べたように人類が古くからガラスにこだわり続けているのはガラスが他の材料には無い特徴を持っているからである。以下にガラスの特徴を述べる。
(1)透明である
物体が透明であるためには「可視光を吸収しない」だけでなく「可視光を散乱しない」ことが必要である。ガラスを構成する主成分であるSiO2やB2O3,Al2O3等は可視光を吸収せず、また結晶質固体で散乱の原因となる結晶粒界が存在しないため、ガラスは可視光域で透明である。ガラス以外の無機固体材料で透光性を持つのは単結晶と特殊なセラミックスのみであり、それ故ガラスは窓材や容器、光学材料として広く用いられている。
(2)成形しやすい
ガラスの粘度は温度の上昇にともない連続的に変化するので、温度を制御することにより加工の容易な柔らかさにすることが可能である。そのため吹く、プレスする、引き伸ばす等の様々な加工が可能である。
(3)組成・物性の自由度が高い
結晶では一定の化学組成比でなければ一様な固体が得られないが、ガラスは非晶質故に多くの場合、相当の組成変化を与えても一様なガラスが得られる。そのため種々の物質をガラスに混入したりガラスの組成を操作して物性値を制御することが可能である。
着色ガラスはこの特性を利用しており、種々の金属元素を添加する事で様々な色のガラスが得られる。
(4)熱的・化学的に安定
多くのガラスはSiO2を主成分としているため酸や有機溶媒などに侵されず、また酸化物であるため高温でも安定である。従って長期使用上、寸法安定性や信頼性が高い。
4. ガラスの製造法
4.1 高温溶融法
最も古典的なガラスの作り方であり、酸化物,炭酸塩,水酸化物等の原料を高温で溶融し急冷してガラスを得る。我々が日常目にするガラスはすべてこの方法で作られている。溶融のための坩堝としては白金,白金-ロジウム,金などの貴金属やアルミナやシリカなどの酸化物の坩堝が主に用いられ、不活性雰囲気で溶融する場合には炭素坩堝も用いられる。加熱の熱源としては電気抵抗加熱や融体への直接通電及びガス等の燃焼加熱が用いられる。
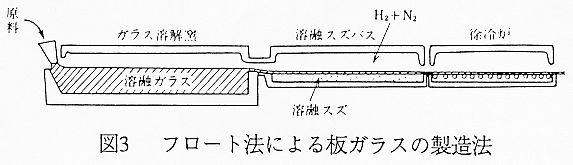
現在の板ガラスの製造法は大変興味深いので特に紹介しておこう。古くは板ガラスを作るためには宙吹きで球状にしたガラスを切り開いて平板を得ていた。またごく最近まで溶融状態からガラス平板を引き上げる方法が標準的な板ガラス製造法として用いられていた。このような板ガラスは表面の平滑性が悪く、生産性も決して高くはなかった。1952年にイギリスのピルキントン社で開発されたフロート法は図3のような方法で平滑性の高い板ガラスを大量に製造する方法であり、現在主流になっている製造法である。フロート法は融液を溶融スズの上に流し、そのまま固化させる方法で板ガラスの両面はガラスの自由表面とガラス/スズの界面であるため研磨せずに平滑面が得られる。
4.2 気相合成法
この方法は液体原料のSiCl4などを気化させ、酸水素炎で酸化させてシリカガラスなどを作成する方法である。反応は次式のような高温酸化反応である。
SiCl4+O2+2H2 → SiO2+4HCl
この反応で得られた微細なSiO2のガラスの粒子の堆積物をさらに高温で焼結してガラスを得る。気相合成法では液体原料を使用するため蒸留等により超高純度の原料を得られること、坩堝を使用しないため坩堝からの汚染がない等の理由から超高純度のガラスが得られる。
4.3 ゾルーゲル法
ゾルーゲル法は液体原料から高温溶融を経ずにガラスを作成する方法として近年注目されている方法である。原料としては主に有機金属化合物(金属アルコキシド等)が用いられる。一例としてテトラエトキシシラン
Si(C2H5O)4を原料とする場合を簡単に述べる。
テトラエトキシシラン Si(C2H5O)4,エタノール,水を混合し、保持すると次式に示すようなテトラエトキシシランの加水分解・脱水縮合により透明なゲルが得られる。
Si(C2H5O)4+4H2O → Si(OH)4+4C2H5OH (加水分解反応)
Si(OH)4 → SiO2+2H2O (脱水縮合反応)
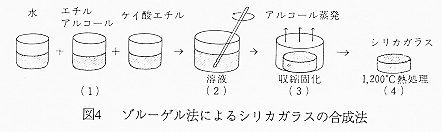
得られたゲルからエタノール、水を蒸発させて収縮固化させ、さらに高温で熱処理するとシリカガラスが得られる。この過程を示したのが図4である。
ゾルーゲル法では溶融過程を経ないため、旧来ガラス中に分散する事が不可能であった各種有機物を容易にガラス中に分散できるため、機能性有機分子の無機ホスト材料として注目されている。
5. ガラスの種類
5.1 酸化物ガラス
我々が日常目にするガラスは全て酸化物から成っており、その多くはケイ酸塩ガラスである。シリカ(SiO2)は単独でガラス化し、シリカガラスとなる。シリカガラスは耐化学性、耐熱・耐熱衝撃性、紫外線透過性など多くの点で優れており、代表的な特殊ガラスである。板ガラスやびんガラスのような実用ガラスの多くは多成分系のケイ酸塩ガラスであり、シリカに種々の酸化物(Na2O,CaO,Al2O3・・・)を添加して溶融温度を下げつつ、各添加物の特徴を反映させている。表2に代表的な実用ガラスの組成を示す。
B2O3を主成分とするホウ酸塩ガラスはケイ酸塩ガラスに比べて溶融温度が低く作り易いが、耐化学性に劣るため特殊な用途にのみ用いられる。用途としては中性子線吸収ガラスや接着用ガラスなどである。
この他、P2O5,GeO2,TeO2,V2O5等を主成分とするガラスがある。
5.2 非酸化物ガラス
硫黄,セレン,テルルの化合物を総称してカルコゲン化物といい、これらで作られるガラスをカルコゲン化物ガラスと呼ぶ。カルコゲン化物ガラスの特徴は赤外光の透過性が高い(可視域では不透明)、電子伝導性の半導体であり光電効果を示す等があり、赤外線透過材料や半導体スイッチング素子等に用いられる。
As2S3,GeS2,As2Se3などを主成分とする。
またフッ素,塩素,臭素の化合物から得られるガラスをハロゲン化物ガラスと呼ぶ。ハロゲン化物ガラスの特徴は赤外透過性が高い、フォノンエネルギーが小さい等があり、赤外線透過材料や蛍光材料としての希土類イオンのホスト等に用いられる。
ZrF4,BaF2,AlF3等の複数成分から成るガラスが主流である。これらガラスの溶融は不活性ガスや真空雰囲気下で行われる。
6. 機能性ガラス
近年、従来の板ガラスやびんガラス等と異なり、新しい機能を持ったガラスが得られており、それらを総称して機能性ガラスまたはニューガラスと呼ばれる。機能性ガラスには各種の機能を備えたものがあり、以下その代表的な材料について解説する。
6.1 光学ガラス
光学ガラスは最初の機能性ガラスといえる。光学ガラスは19世紀にドイツで発展し、その発展に寄与したエルンスト・アッベ,オットー・ショット,カール・ツァイスの名
は余りにも有名である。現在の光学ガラスのカタログには図5の様に実に様々な種類のガラスが掲載されている。これだけ多種多様な物性値を持つ材料は他に見当らないが、これは色収差を克服するために作り出されたものである。プリズムで光が7色に分かれるのと同様、レンズを通過した光も僅かながら波長による光路の差が現れる(色収差)。この現象は屈折率が波長により異なるためで、この屈折率の波長依存性を分散と呼ぶ。カメラや望遠鏡などの設計では収差を抑えるため、屈折率や分散の異なる複数のレンズが組み合わされている。
6.2 光ファイバ-
光ファイバーは酸化物ガラスの可視・近赤外領域での透明度を極限まで高めた材料である。その透明度は現在、波長1.55μmの光に対して
0.2dB/kmであり、これはファイバー中を1km透過した後の光の強度が約5%しか減衰しないことに相当する。光ファイバーはのように半径方向に屈折率分布を持っており、高い屈折率を持つ中心部(コア)と低い屈折率の周辺部(クラッド)から成る。
屈折率分布の形状は図6の様に階段状のステップインデックス型と連続分布のグレーデッドインデックス型に分けられる。ファイバーの断面に異なった角度で入射した光は図6で示されるようにステップインデックス型ではコア・クラッド界面で全反射されながら、
グレーデッドインデックス型では進行方向を連続的に変化されながら伝播される。 光ファイバーは気相合成により作製されており、中でもVAD法(Vapor
phase Axial Deposition)はファイバー製造法として最も優れた方法である。原料にはSiCl4,GeCl4等が用いられ、これらをH2-O2火炎内で燃焼させ、GeO2及びSiO2の堆積物が得られる。これが多孔質プリフォームであり、GeO2濃度はプリフォームの中心部に行くほど高くなるように原料が供給されているため、後にファイバーとしたときに中心部ほど屈折率が高くなる。プリフォームはヒーターで加熱しつつ引き上げられ、その過程で多孔質であったプリフォームは緻密で透明なガラス棒となる。
これを細く引き伸ばしてファイバーを得る。
6.3 屈折率分布型レンズ
通常のレンズは屈折率の均一なガラスに凸または凹の球面を与えて光を屈折させているが、場所により屈折率の異なるガラスを用いれば球面研磨をしなくてもレンズとしての機能を果たすことになる。このような屈折率分布を持つレンズをgradient
index lensと呼ぶ。
ガラス中に屈折率分布を作るためにはイオン交換によるのが一般的である。ガラスを構成するイオンのうち1価のイオンは比較的容易にイオン交換できる。そこで屈折率を高めるような1価イオン(通常タリウムを用いる)を含むガラスを溶融し、直径数mmの
円柱にする。これを他の1価イオン(カリウム等)を含む溶融塩に浸漬する。すると表
面からイオン交換が進行し、中心部に近いほど元のイオン(タリウム)の濃度が高いため、中心部から表面にかけて連続的な屈折率変化を持つレンズが得られる。
屈折率分布型レンズの用途としてはレンズアレイがある。レンズアレイでは個々のレンズの像を重ね合わせて一体の像を得られるという特徴がある。複写機にレンズアレイを使うと、これまで鏡やレンズを組み合わせていた所を1個のレンズアレイで代用できるため装置を小型化できる。最近の複写機やファクシミリの小型化にはこのレンズアレイが大きな役割をはたしている。
6.4 レーザーガラス
固体レーザー材料としてはルビーやNd:YAG等の単結晶及びNd等の希土類元素をドープしたガラスが用いられている。単結晶のレーザーの場合には光学的に均一で大型の単結晶を得るのは難しいという欠点がある。この点ガラスレーザーの場合には大型で均一な材料が得られ、成形も容易であるため、大出力のレーザー材料として特に核融合用レーザーとして利用されている。
レーザーのように強力な光では物質の屈折率は光の電場に依存して変化し、このため物質中で光が直進せず、一点に集束する自己集束現象が起こり得る。レーザー材料中で自己集束が起こるとそれ自身が破壊されるため、ガラスレーザー用の材料としては非線形屈折率が小さく、自己集束が起こりにくいリン酸塩系ガラスが主に用いられている。
6.5 フォトクロミックガラス
物質が光によって着色する現象をフォトクロミズムといい、サングラスなどに実用化されている。このガラスは感光性の物質をガラス中に分散させており、感光性の物質としては写真などと同様にハロゲン化銀が用いられている。
ハロゲン化銀に光が当たると次式のような分解反応が進行する。
AgX → Ag0+X0 (Xは多くの場合、塩素)
生成したAg0は互いに集合してコロイドを形成し、銀コロイドが光を吸収するため着色する。写真フィルムの場合、生成したX0はフィルムのゼラチン層中にトラップされるため一度生成した銀コロイドは元に戻らない。一方、ガラス中では生成したAg0とX0はそのまま保持されるため、暗所では逆反応が進行し透明に戻る。感光性のサングラスはこの現象を利用している。
6.6 各種基板用ガラス
近年の磁気ディスクや光磁気ディスクなどの記録媒体の記録密度の向上は目ざましく、それに伴ってディスク用基板の精度に対する要求も厳しくなっている。基板用材料としてはアルミニウム合金が広く用いられてきたが、ディスク表面の平滑性や高弾性の点で優れるガラス基板が利用され始めている。
また半導体製造用のフォトマスクはミクロンオーダーの回路パターンを半導体表面に紫外線で焼き付けるため、低熱膨張で紫外線透過性に優れることが要求される。このためシリカガラスやホウケイ酸塩系のガラスが用いられている。
6.7 電気伝導性ガラス
電気伝導性のガラスには大別して二種類あり、通常のガラス表面に透明導電膜を付けたガラスとガラス自体が電気伝導性をもつガラスである。
ガラス表面にIn2O3+SnO2またはSnO2+Sb2O3の薄膜をコーティングした透明電極は液晶表示板などに広く利用されている。
一方、ガラス自体が導電性を持つガラスがあり、特にAgI-Ag2O系について多くの研究が行われている。このようなガラス中はAg+イオンの移動により導電性を示すためイオン伝導性ガラスと呼ばれる。電気伝導率は最高2×10-2S・cm-1程度であり、これは食塩水と同程度である。(窓ガラスは10-13程度)
6.8 多孔質ガラス
ある種のガラスは組成の異なる二種類のガラス相に分相する。特にNa2O-B2O3-SiO2系のガラスでは、かなり広い組成範囲において、Na2O-B2O3相とSiO2相の2相に分相することが知られている。
分相によって生成した第二相を溶解・除去するとその部分が空隙となり、微細な空隙を多数有するガラスが出来る。これが多孔質ガラスである。図10に多孔質ガラスの代表的な製法を示す。
所定組成のNa2O-B2O3-SiO2系ガラスを作成し、所望の形状に成形する。このガラスを熱処理するとNa2O-B2O3相とSiO2相に分相した図10(b)のような分相ガラスが得られる。分離相の大きさは、熱処理の時間、温度によって制御できる。分相ガラス中のNa2O-B2O3相はSiO2相に比べて耐化学性が著しく低いので、これを酸または熱水で溶出処理するとSiO2骨格を持つ多孔質体が得られる(図10(c))。
このようにして得られる多孔質ガラスは次のような特徴を持っている。
・径が数nm~数μmの貫通細孔を無数に有し、比表面積も最大数百m2/gと大きい
・細孔径や比表面積を熱処理過程で容易に制御できる
・高ケイ酸質であるため耐化学性・耐熱性が優れている。
多孔質ガラスの用途としては各種の分離膜,無機触媒及び酵素の担体などがある。
6.9 結晶化ガラス
ガラスにおける結晶化は前項で述べた分相と同様にガラスの透光性を損なうものとして忌避されてきた。しかし近年、ガラス中に結晶を析出させることによりガラス単独では得られない特性を持つ材料が開発されており、これらを結晶化ガラスと呼ぶ。
以下に結晶化ガラスの実用例をあげる。
(1)マシナブルガラス
ガラスは脆いため金属の様な切削加工を行うと、加工によって生じた亀裂が材料全体に伝播し破壊に至る。結晶析出を利用してこの欠点を克服したのがマシナブルガラスである。代表的なマシナブルガラスである「マコール」はガラス中に雲母の微結晶を析出させ、雲母のへき開性を利用して加工により生じたクラックの進展を妨げている。
(2)化学切削ガラス
貴金属を加えて溶融したガラスでは光を照射してから加熱すると光を受けた部分のみに貴金属のコロイドが生成し、これが結晶核となってガラス中に結晶が析出する。そこでフォトマスクを通して露光する事によりガラス中の任意の部分のみにLi2O・SiO2のような化学的耐久性の低い結晶を析出させ、その結晶を酸などで溶解すると機械加工以上の精密加工が可能となる。
6.10 耐アルカリガラス
先にガラスは耐化学性が高いと記したがアルカリには非常に弱く、pH9以上では溶解する。これはガラス中のSi-O-Si結合がOHにより切断されHSiO3-やSiO32-として溶解するためである。この性質を改善したのが耐アルカリガラスでありNa2O-ZrO2-SiO2系などケイ酸塩ガラスにZrO2やTiO2を添加したガラスが用いられている。
用途としては、これらガラスの繊維をセメントと複合させたガラス繊維強化セメント(GRC)などがある。GRCは軽量で曲げ強度や耐衝撃性に優れているため建材として期待されているが、セメント中はpH12以上の強アルカリ性であるため耐アルカリガラス繊維が用いられる。
6.11 放射性廃棄物固化ガラス
高レベル放射性廃棄物の処理法の一つとしてガラス固化法がある。この方法は90Sr,137Cs等の放射性廃棄物をガラス原料とともに溶解しガラス化して保管または地中に埋没する方法である。このようなガラスは以下のような特性が要求される。
・多量の放射性廃棄物を含有し、かつ機械的強度や耐化学性が高い
・長期間放射性廃棄物の発する放射線や高熱に曝されても形状や耐化学性の変化を
起こさない
・溶融温度が比較的低いこと(高温で溶融すると放射性元素が揮散するため)
上記の条件を満足するため、ホウケイ酸系のガラスが主に用いられている。放射性廃棄物固化用ガラスは耐化学性が高く、種々の物質を多量に含有できるというガラスの特徴を利用したものとして興味深い。


